БУДЕТ
кращению Любовь имеет место в человеческом сердце от рождения. Любовь матери причин этого роста. Мы любим наш отец, мать, брат и друг, а когда мы в школу, мы любим наших учителей. Между прочим, мы любим нашу страну, как наши мнения получить больше. Как наши мнения получить больше и больше, мы любим мир, в котором мы живем, и людей, живущих в нем. Права любви является очень важным ощущением, и она связывает людей на жизнь. Давайте любить, быть любимыми, и пусть наши сердца будут полны любви.
Если человек является самым ценным существом в мире Наиболее ценные люди - это тот, кто является добродетельным. Если первое условие быть добродетельный - любовь, второй - уважение. Человек должен сначала проявить уважение ему / ей, должно быть гармоничным с его идеями и не должны терять истину. Никто не приветствуем тех, кто вдруг одумались и кто говорит, черный, на которые он / она говорит белым днем раньше. Такого рода люди не могут взглянуть в зеркало без красного. Люди упрочнения отношению к самим себе, проявляя уважение к другим. Мы не должны разговоров о всех, кого разорвать сердце, и не следует говорить серьезно.
Для спорта - это наилучший способ уменьшить стресс повседневной жизни. Чтобы быть активным, ходить, заниматься гимнастикой, запустить ... чистых клеток в организме человека. Людей, которые очищали от грязи более энергичным и сыпь, и это делает людей держать молодых и энергичные. Если мы сделаем гимнастику каждый день и делаем это нашим привычкам, мы понимаем, что свободного времени будет трудно жить нам.
Права мозг играет очень важную роль. Она образуется, что ли нести основную роль в жизни этапом или будут дополнительные. Когда мозг начинает реализовать некоторые вещи, он начинает действовать автоматически. Например, он хочет прав, в мозг она принесла главная роль. Знания необходимые для этого вещь. Наилучшим и наиболее подходящим знания в книгах, и это делает людей хотят прочитать. Когда люди читали, свои мозги получите полную необходимых знаний. Когда уровень получения знания на достаточном уровне, человеческого мозга начнет выдвигать идеи, как плотина в производстве электроэнергии.
Написал : Сердар Илдырым
ERDEMLİ OLMAK
Sevgi insanın kalbinde doğuştan yer etmiştir. Anne sevgisi bunun gelişmesine neden olur. Babamızı severiz, kardeşimizi severiz, arkadaşımızı severiz, okula gider öğretmenimizi severiz, düşüncelerimiz büyüdükçe vatanımızı severiz. Düşüncelerimiz daha da büyüdükçe üstünde yaşadığımız dünyayı severiz ve o dünyada yaşayan insanları severiz. İnsan sevgisi çok önemli bir duygudur ve insanı hayata bağlar. Sevelim, sevilelim, bırakalım kalbimiz sevgiyle dolsun.
Dünyadaki canlıların en değerlisi insansa, insanların en değerlisi erdemli olandır. Erdemli olmanın ilk koşulu sevgiyse, ikincisi saygıdır. İnsan önce kendine saygı duymalıdır. Fikirleriyle barışık olmalıdır. Doğruluktan şaşmamalıdır. Durup dururken fikir değiştiren, bugün beyaz dediğine yarın siyah diyeni kimse alkışlamaz. Böyleleri aynaya yüzü kızarmadan bakamaz. İnsan kendine olan saygısını başkalarına saygı duyarak pekiştirir. Başkasının arkasından konuşmamalı, kimsenin kalbini kırmamalı, kötü söz söylememelidir.
Spor yapmak günlük hayatın sıkıntısını en aza indirgemek için biçilmiş kaftandır. Hareketli olmak, yürümek, jimnastik yapmak, koşmak…vücudumuzun hücrelerine birikmiş olan kiri temizler. Kirden arınan insan daha canlı ve atak olur. Bu da insanın genç ve dinç kalmasını sağlar. Her gün jimnastik yaparsak ve bunu alışkanlık haline getirirsek geçen zamanın bizi yaşlandırmak için zorlanacağını fark ederiz.
İnsan beyni çok önemli bir rol üstlenir. Hayat sahnesinde başrolde mi oynayacağın yoksa figüran mı kalacağın orada şekillenir. Beyin bazı şeyleri fark etmeye başladığında kendiliğinden harekete geçer. Örneğin, kafatası içinde durduğu insanın başrolde oynamasını istemektedir. Bunun için gerekli olan şey bilgidir. En iyi ve en doğru bilgi kitaptadır. Bu, insanda okuma isteği yaratır. İnsanın okuması beynin gerekli bilgilerle dolmasını sağlayacaktır. Dolum seviyesi yeterli düzeye ulaştığında, barajın elektrik üretmesi gibi, insan beyni fikir üretmeye başlayacaktır.
BİYOLOJİ SINIFIM
Biyoloji derslerinize çalışmak için en uygun site
18 Haziran 2014 Çarşamba
RECHTSCHAFFEN SEIN
RECHTSCHAFFEN SEIN
Liebe hat einen Platz in den Herzen des Menschen von der Geburt. Die Liebe einer Mutter veranlaßt dieses zu wachsen. Wir lieben unseren Vater, Mutter, Geschwister und Freund und wenn wir Schule beginnen, lieben wir unsere Lehrer. Übrigens lieben wir unser Land, während unsere Meinungen grösser erhalten. Während unsere Meinungen grösser und grösser erhalten, lieben wir die Welt, die wir innen und die Leute leben, die in ihm leben. Menschliche Liebe ist ein sehr wichtiges Gefühl und sie bindet Leute an das Leben. Lassen Sie uns lieben, zu sein liebte und unsere Herzen, von der Liebe voll zu sein lassen.
Wenn menschliches Wesen das wertvollste Geschöpf in der Welt ist, ist das wertvollste menschliche Wesen das, wer rechtschaffen ist. Wenn der erste Zustand des Seins rechtschaffen Liebe ist, zweite ist Respekt. Ein Mensch Wesen sollte Respekt zu ihm/zu selbst zuerst zeigen, sollte mit seinen Ideen harmonisch sein und sollte nicht die Wahrheit verlieren. Noone applaudiert die, die ihren Verstand plötzlich ändern und die Schwarzes sagen, zu dem er/sie besagtes Weiß der Tag vorher. Diese Arten der Leute können nicht den Spiegel betrachten ohne gehendes Rot. Leute verhärten den Respekt zu selbst, indem sie Respekt zu anderen zeigen. Wir sollten nicht über niemand, Bruch jedermann klatschen Herz und sollten nicht rauh sprechen.
Sport zu tun ist die beste Weise, den Druck des täglichen Lebens zu vermindern. Um aktiv zu sein, zu gehen, Gymnastik, zum Durchlauf zu tun… die Zellen in unseren Körpern säubern. Die Leute, die vom Schmutz sind energischer gereinigt werden und der Hautausschlag und diese Marke Leute halten, jung und kräftig zu sein. Wenn wir die tägliche Gymnastik tun und es unsere Gewohnheit bilden, stellen wir fest, daß die vergehende Zeit die Schwierigkeit hat, zum wir zu altern.
Menschliches Gehirn hat eine sehr wichtige Rolle. Es wird dort gebildet, ob man die Hauptrolle auf Lebenstadium hat oder die Extrakosten ist. Wenn Gehirn beginnt, einige der Sachen zu verwirklichen, fängt es an, automatisch zu fungieren. Zum Beispiel wünscht es den Menschen in dessen Gehirn es, die Hauptrolle zu haben ist. Wissen ist die notwendige Sache für dieses. Das beste und verwendbarste Wissen ist in den Büchern und dieses läßt Leute lesen wünschen. Wenn die gelesenen Leute, ihre Gehirne voll vom notwendigen Wissen erhalten. Wenn das Niveau des Erhaltens des Wissens auf einem genügenden Niveau ist, beginnt menschliches Gehirn, Ideen wie die produzierende Elektrizität einer Verdammung vorzubringen.
Vorbei geschrieben: Serdar YILDIRIM
ERDEMLİ OLMAK
Sevgi insanın kalbinde doğuştan yer etmiştir. Anne sevgisi bunun gelişmesine neden olur. Babamızı severiz, kardeşimizi severiz, arkadaşımızı severiz, okula gider öğretmenimizi severiz, düşüncelerimiz büyüdükçe vatanımızı severiz. Düşüncelerimiz daha da büyüdükçe üstünde yaşadığımız dünyayı severiz ve o dünyada yaşayan insanları severiz. İnsan sevgisi çok önemli bir duygudur ve insanı hayata bağlar. Sevelim, sevilelim, bırakalım kalbimiz sevgiyle dolsun.
Dünyadaki canlıların en değerlisi insansa, insanların en değerlisi erdemli olandır. Erdemli olmanın ilk koşulu sevgiyse, ikincisi saygıdır. İnsan önce kendine saygı duymalıdır. Fikirleriyle barışık olmalıdır. Doğruluktan şaşmamalıdır. Durup dururken fikir değiştiren, bugün beyaz dediğine yarın siyah diyeni kimse alkışlamaz. Böyleleri aynaya yüzü kızarmadan bakamaz. İnsan kendine olan saygısını başkalarına saygı duyarak pekiştirir. Başkasının arkasından konuşmamalı, kimsenin kalbini kırmamalı, kötü söz söylememelidir.
Spor yapmak günlük hayatın sıkıntısını en aza indirgemek için biçilmiş kaftandır. Hareketli olmak, yürümek, jimnastik yapmak, koşmak…vücudumuzun hücrelerine birikmiş olan kiri temizler. Kirden arınan insan daha canlı ve atak olur. Bu da insanın genç ve dinç kalmasını sağlar. Her gün jimnastik yaparsak ve bunu alışkanlık haline getirirsek geçen zamanın bizi yaşlandırmak için zorlanacağını fark ederiz.
İnsan beyni çok önemli bir rol üstlenir. Hayat sahnesinde başrolde mi oynayacağın yoksa figüran mı kalacağın orada şekillenir. Beyin bazı şeyleri fark etmeye başladığında kendiliğinden harekete geçer. Örneğin, kafatası içinde durduğu insanın başrolde oynamasını istemektedir. Bunun için gerekli olan şey bilgidir. En iyi ve en doğru bilgi kitaptadır. Bu, insanda okuma isteği yaratır. İnsanın okuması beynin gerekli bilgilerle dolmasını sağlayacaktır. Dolum seviyesi yeterli düzeye ulaştığında, barajın elektrik üretmesi gibi, insan beyni fikir üretmeye başlayacaktır.
Liebe hat einen Platz in den Herzen des Menschen von der Geburt. Die Liebe einer Mutter veranlaßt dieses zu wachsen. Wir lieben unseren Vater, Mutter, Geschwister und Freund und wenn wir Schule beginnen, lieben wir unsere Lehrer. Übrigens lieben wir unser Land, während unsere Meinungen grösser erhalten. Während unsere Meinungen grösser und grösser erhalten, lieben wir die Welt, die wir innen und die Leute leben, die in ihm leben. Menschliche Liebe ist ein sehr wichtiges Gefühl und sie bindet Leute an das Leben. Lassen Sie uns lieben, zu sein liebte und unsere Herzen, von der Liebe voll zu sein lassen.
Wenn menschliches Wesen das wertvollste Geschöpf in der Welt ist, ist das wertvollste menschliche Wesen das, wer rechtschaffen ist. Wenn der erste Zustand des Seins rechtschaffen Liebe ist, zweite ist Respekt. Ein Mensch Wesen sollte Respekt zu ihm/zu selbst zuerst zeigen, sollte mit seinen Ideen harmonisch sein und sollte nicht die Wahrheit verlieren. Noone applaudiert die, die ihren Verstand plötzlich ändern und die Schwarzes sagen, zu dem er/sie besagtes Weiß der Tag vorher. Diese Arten der Leute können nicht den Spiegel betrachten ohne gehendes Rot. Leute verhärten den Respekt zu selbst, indem sie Respekt zu anderen zeigen. Wir sollten nicht über niemand, Bruch jedermann klatschen Herz und sollten nicht rauh sprechen.
Sport zu tun ist die beste Weise, den Druck des täglichen Lebens zu vermindern. Um aktiv zu sein, zu gehen, Gymnastik, zum Durchlauf zu tun… die Zellen in unseren Körpern säubern. Die Leute, die vom Schmutz sind energischer gereinigt werden und der Hautausschlag und diese Marke Leute halten, jung und kräftig zu sein. Wenn wir die tägliche Gymnastik tun und es unsere Gewohnheit bilden, stellen wir fest, daß die vergehende Zeit die Schwierigkeit hat, zum wir zu altern.
Menschliches Gehirn hat eine sehr wichtige Rolle. Es wird dort gebildet, ob man die Hauptrolle auf Lebenstadium hat oder die Extrakosten ist. Wenn Gehirn beginnt, einige der Sachen zu verwirklichen, fängt es an, automatisch zu fungieren. Zum Beispiel wünscht es den Menschen in dessen Gehirn es, die Hauptrolle zu haben ist. Wissen ist die notwendige Sache für dieses. Das beste und verwendbarste Wissen ist in den Büchern und dieses läßt Leute lesen wünschen. Wenn die gelesenen Leute, ihre Gehirne voll vom notwendigen Wissen erhalten. Wenn das Niveau des Erhaltens des Wissens auf einem genügenden Niveau ist, beginnt menschliches Gehirn, Ideen wie die produzierende Elektrizität einer Verdammung vorzubringen.
Vorbei geschrieben: Serdar YILDIRIM
ERDEMLİ OLMAK
Sevgi insanın kalbinde doğuştan yer etmiştir. Anne sevgisi bunun gelişmesine neden olur. Babamızı severiz, kardeşimizi severiz, arkadaşımızı severiz, okula gider öğretmenimizi severiz, düşüncelerimiz büyüdükçe vatanımızı severiz. Düşüncelerimiz daha da büyüdükçe üstünde yaşadığımız dünyayı severiz ve o dünyada yaşayan insanları severiz. İnsan sevgisi çok önemli bir duygudur ve insanı hayata bağlar. Sevelim, sevilelim, bırakalım kalbimiz sevgiyle dolsun.
Dünyadaki canlıların en değerlisi insansa, insanların en değerlisi erdemli olandır. Erdemli olmanın ilk koşulu sevgiyse, ikincisi saygıdır. İnsan önce kendine saygı duymalıdır. Fikirleriyle barışık olmalıdır. Doğruluktan şaşmamalıdır. Durup dururken fikir değiştiren, bugün beyaz dediğine yarın siyah diyeni kimse alkışlamaz. Böyleleri aynaya yüzü kızarmadan bakamaz. İnsan kendine olan saygısını başkalarına saygı duyarak pekiştirir. Başkasının arkasından konuşmamalı, kimsenin kalbini kırmamalı, kötü söz söylememelidir.
Spor yapmak günlük hayatın sıkıntısını en aza indirgemek için biçilmiş kaftandır. Hareketli olmak, yürümek, jimnastik yapmak, koşmak…vücudumuzun hücrelerine birikmiş olan kiri temizler. Kirden arınan insan daha canlı ve atak olur. Bu da insanın genç ve dinç kalmasını sağlar. Her gün jimnastik yaparsak ve bunu alışkanlık haline getirirsek geçen zamanın bizi yaşlandırmak için zorlanacağını fark ederiz.
İnsan beyni çok önemli bir rol üstlenir. Hayat sahnesinde başrolde mi oynayacağın yoksa figüran mı kalacağın orada şekillenir. Beyin bazı şeyleri fark etmeye başladığında kendiliğinden harekete geçer. Örneğin, kafatası içinde durduğu insanın başrolde oynamasını istemektedir. Bunun için gerekli olan şey bilgidir. En iyi ve en doğru bilgi kitaptadır. Bu, insanda okuma isteği yaratır. İnsanın okuması beynin gerekli bilgilerle dolmasını sağlayacaktır. Dolum seviyesi yeterli düzeye ulaştığında, barajın elektrik üretmesi gibi, insan beyni fikir üretmeye başlayacaktır.
Wie man Fremde macht
Wie man Fremde macht
Wolfgang Kaschuba
Mit diesem Kongress wird ein wichtiger und mutiger Schritt im Dialog der Religionen
gemacht, der aus historischen wie aktuellen Gründen immer dringlicher wird. Denn gerade in
Europa war der Raum der Religionen stets ein zentrales Konflikt- und Kraftfeld – ich erinnere
nur an die Geschichte der Kreuzzüge, Hexenverfolgungen, Konfessionskriege und
Judenverfolgungen unter christlichen Vorzeichen. Und er ist bis heute ein Konfliktfeld
geblieben. Mit Konflikten etwa auch zwischen christlichen Konfessionen und jüdischer
Religion. Auch wenn konservative Kreise gegenwärtig gerne so tun, als sei der Islam der
„Störenfried“ in einem Europa der Ökumene und des friedlichen Miteinander.
Mein Titel: „Wie man Fremde macht“ will dies aufnehmen: jene europäische Tradition der
„Integration durch Differenz“, der Ausbildung von inneren Wir-Gefühlen durch die
Abgrenzung und Schuldzuweisung nach außen. Als religiöse, als ethnische oder nationale
„Fremdheit“ apostrophiert: Es ist ein altes europäisches Machtspiel, das mit solchen
Differenz-Konstruktionen vollführt wird. Manchmal geschah dies nur spielerisch-diskursiv,
etwa in Gestalt von wechselseitigen Stereotypen und Karikaturen; manchmal aber auch bis an
die Gegenwart heran aggressiv und blutig von den dramatischen Kriegen und „ethnischen
Säuberungen“ im ehemaligen Jugoslawien bis zu einzelnen Gewaltakten im Namen von
Nation, Religion oder regionaler Autonomie.
Mein Feld, die Ethnologie, war an dieser Politik der „Identität durch Differenz“ in der
Vergangenheit aktiv beteiligt. So entwarf die Volkskunde im 19. Jahrhundert als Wissenschaft
von der „eigenen Kultur“ wirksame ethnische und nationale Selbstbilder. Und die
Völkerkunde als Wissenschaft von den „fremden Kulturen“ begleitete koloniale Eroberungen
und rechtfertigte mit den entsprechenden Bildern die Essentialisierung von Ethnie und Nation,
auch von Christentum und „Whiteness“. Deshalb bemühen wir uns heute auch, diese
wissenschaftliche Schuld aufzuarbeiten und abzutragen, die im historischen Kontext von
Nationalismus, Kolonialismus und kulturellem wie religiösem Fundamentalismus aufgetürmt
wurde. Gerade auch in Deutschland und vor dem Hintergrund deutscher Geschichte, in die
offenbar eine spezifisch deutsche Tradition der „Fabrikation des Fremden“ eingeschrieben ist.
Wolfgang Kaschuba
Mit diesem Kongress wird ein wichtiger und mutiger Schritt im Dialog der Religionen
gemacht, der aus historischen wie aktuellen Gründen immer dringlicher wird. Denn gerade in
Europa war der Raum der Religionen stets ein zentrales Konflikt- und Kraftfeld – ich erinnere
nur an die Geschichte der Kreuzzüge, Hexenverfolgungen, Konfessionskriege und
Judenverfolgungen unter christlichen Vorzeichen. Und er ist bis heute ein Konfliktfeld
geblieben. Mit Konflikten etwa auch zwischen christlichen Konfessionen und jüdischer
Religion. Auch wenn konservative Kreise gegenwärtig gerne so tun, als sei der Islam der
„Störenfried“ in einem Europa der Ökumene und des friedlichen Miteinander.
Mein Titel: „Wie man Fremde macht“ will dies aufnehmen: jene europäische Tradition der
„Integration durch Differenz“, der Ausbildung von inneren Wir-Gefühlen durch die
Abgrenzung und Schuldzuweisung nach außen. Als religiöse, als ethnische oder nationale
„Fremdheit“ apostrophiert: Es ist ein altes europäisches Machtspiel, das mit solchen
Differenz-Konstruktionen vollführt wird. Manchmal geschah dies nur spielerisch-diskursiv,
etwa in Gestalt von wechselseitigen Stereotypen und Karikaturen; manchmal aber auch bis an
die Gegenwart heran aggressiv und blutig von den dramatischen Kriegen und „ethnischen
Säuberungen“ im ehemaligen Jugoslawien bis zu einzelnen Gewaltakten im Namen von
Nation, Religion oder regionaler Autonomie.
Mein Feld, die Ethnologie, war an dieser Politik der „Identität durch Differenz“ in der
Vergangenheit aktiv beteiligt. So entwarf die Volkskunde im 19. Jahrhundert als Wissenschaft
von der „eigenen Kultur“ wirksame ethnische und nationale Selbstbilder. Und die
Völkerkunde als Wissenschaft von den „fremden Kulturen“ begleitete koloniale Eroberungen
und rechtfertigte mit den entsprechenden Bildern die Essentialisierung von Ethnie und Nation,
auch von Christentum und „Whiteness“. Deshalb bemühen wir uns heute auch, diese
wissenschaftliche Schuld aufzuarbeiten und abzutragen, die im historischen Kontext von
Nationalismus, Kolonialismus und kulturellem wie religiösem Fundamentalismus aufgetürmt
wurde. Gerade auch in Deutschland und vor dem Hintergrund deutscher Geschichte, in die
offenbar eine spezifisch deutsche Tradition der „Fabrikation des Fremden“ eingeschrieben ist.
İngilizce Makale -3- Nuclear Energy Is Life
In the text “The Benefits of Nuclear Energy”, Colomby Bruno (2008) supports that “is the only soource of enery that can replace a significant part of the fossil fuels (coal, oil and gas) which massively pollute the athmosphere and contribute to the greenhouse effect” (para.1). Using gas, oil or coal for human needs have been forming may problems for whole the world as these structures pollute air and environent. I completely support the author’s positive opinions about nuclear poer due to it’s certain advantages and positive effects for nature.
To begin with, about the cost and stabelity sides of Nuclear power. When coal costs and usage in the past is thught, there will clearly appear that coal costs have been increasing by year by which makes people in a difficult stuation; however, nuclear power is not like coal or others. Firstly, nuclear power is the best source for our budget. Hw can i say this, certainly? There is a research about this subject, OECD study. There are thirteen countries which use whole types of energies in a year (2001), in this study. The rsult is so surprised me that there is a huge difference between nuclear power, coal and gas costs. To illustrate, in Belgium, nuclear power cost is 6.1 c/kWh while coal is 8.2 c/kWh and gas is 9.0 c/kWh. Morever, this difference is bigger in China is that while nuclear power cost is 3.6 c/kWh, coal is 5.5 c/kWh (table 4-1). These results show that nuclear energy is cheaper tha others therefore people can use it safely and easly for their nature and especially budget. Morover, nuclear power limits the electricity cost, that is, when people use different amounts electricity. In Finland, a research was done in 2003 about ths. Result of this research shows that there is clear difference between nuclear powr and other types of energy. While gas is used, electricity price increases to 3.92; however, nuclear power decreases this price to 2.37. The most interesting result of the study is that wind using makes prices 5.01. Can you see the huge difference? Secondly, nuclear energy is stable ,that is, it is useful and safe for nature of human. Marvin Fertel, the Nuclear Energy Institute’s Chef Nuclear Officer, in his talks about the Clean Air and Climate Change of the US, he says that they thought public health and safety . In addition to this, they try to avoid environment pollution. His statement is really absorbing that nuclear plants provides consumers and businesses with a high degree of forward prices stability.
After the cost and stability sides of nuclear power, Comby says tht an increasing number of environmentalists are now changing their minds about nuclear energy as there are good , solid, scentific and environmental reasons to be in favor of nuclear energy. This is certainly true true as people will not use gas r coal, if they think the huge disadvantages of these energy sources. As people use too much the land needed by Earth to regulate it’s climate and cemistry. For example, a car consumes 10 to 30 times as much as its drivers; when we imagine the extra formland required to feed the appetite of cars, this will be more complex. Lovelock says “…, let us use the small input from renewables sensibly, but only one immediately avaible source does not cause global warng and that is nuclear energy. ”(2004, p.2)That is true because we use the natural gas instead of coal or oil releases, half of much carbondioxide forms. After nuclear power’s price , stable and environmental part, there is a good point for nuclear enery that science, that is nuclear energy is removable. We can product them in different and difficult conditions, too, since their source does not finish. In addition to this, NMD reports show that different amount of energy. For example, gas produces 39 mj/kg while uranium which is the main source of nuclear power produces 24.000.000 mj/kg. (Ünalan, 2008, p.3) Can you see the huge difference between the energy sources? Science comes in this point. We can produce as a huge amount of energy from uranium. In addition to these points, nuclear energy can be used by using science for a country’s needs. To illustrate, China,the most crowded country in the World, plans it’s economy and energy sources. China plans to solve it’s energy problem by paying atention to nuclear energy. To do this, Chineese scientists have developed their nuclear power production technlogy. Morever, they say that thy will not need to any other source from nuclear energy in 3000 years if they use nuclear energy plants. (“China tries to,” 2011) Therefore, this shows people that nuclear energy should be used more efficiently.
To sum up, nuclear power is the most useful source because of it’s cost, environmetalist side and edtable side for science. To make people more healthy and safer, we should use nuclear power despite coal, or gas because nuclear energy is life.
İngilizce Makale -2- TURKISH IS ENOUGH FOR US
Not only in these days, but also in the past, a country’s development level have been depend on its level of education which is defined by Crawley and Ashby as teaching somebody about things like reading, writing and mathematics at school or college (1994, p. 106). In Turkey, after students finish high school, they start university where they learn their jobs efficiently. During university years, youngs develop themselves and learn what they want. When this feature of universities’ is thought, there appear two types of schools. While students get their whole education in English in one of them, students get their education in their native language, Turkish, in other type. A result can be clearly seen that students should not be forced to study their departments in English in Turkey because of negative effects of English based education.
Using English as instruction language in Turkey can help students to understand and write academic essays in English for their departments. That is, when they use English in their department continuously, they know English as Turkish too. However, when they do not write any essays in Turkish, Turkey may not achieve academic successes as students write their essays, reports, summaries and outlines in English while they think in Turkish. Not using Turkish in department lessons, they may forget grammar and basic concepts of Turkish and lose their ability of producing Turkish literatures.
Taking education in English forms different problems for university students. The first problem for students is that they may lose their important senses due to their education language. They may lose their not only personal senses such that learning passion or self-confidence, but also their academic senses such that criticism or command abilities during their education life. When they get their subjects in English, they must do two difficult jobs simultaneously. While they listen and translate the topic which their instructor tell them, they should be able to understand what are the main points of the subject and where they should pay attention. As a result of this, they lose their passion for learning the subject. Moreover, they may lose their self-confidence since they may not follow the topic efficiently. That is, they may lose their attention to subject in lesson then they may not be able to catch the lecture again which can make them demoralized. For this reason, they can think that they would not pass the exam ad would fail it. Students may lose their valid academic senses due to their lecture language. In other words, they may not criticize the topic efficiently while they use English in their lecture hours continuously. As when one lose a main point of the topic, s/he may miss whole valid points of topic. Analyzing and criticizing abilities are born with command ability which makes the lessons more understandable for students. Lack command ability may make a student be failed. “ Our clever students are lack of analyzing, commanding and criticizing abilities for Math, Physic or Chemistry lessons which need to command, criticism and analyses. “ (Demirören, 2002, p.1)
The second problem due to their education language is that students cannot learn easily and clearly their department courses .While students sometimes cannot learn some courses in their native languages how can they learn them in English ? Demirören supports my observation in his thesis. In summary, he says that students only want to pass their exams with high grades so they do not try to take the main points of the lesson, which makes them with poor education. (2002, p.1) One can learn a job’s basic elements and develop new things about her/his job if s/he gets education in her/his native language as people should know native terms of their jobs’ but also English versions. Sinanoğlu thinks that a student can develop himself in his job and career life safely if he gets his education in his own language. (2006, p.12) Students may get English courses in their free times such as summer holidays or after lecture hours.
In conclusion, while English Based Education may help students in some ways, it has negative effects on students more. Due to its privative effects on students’ basic senses and learning process, English should not be the medium instruction language in Turkish universities. Despite these applications, students should be oriented for applying language courses in summer holidays not in university education as obligatory. Not only its grammar, but also its meaningful structure, Turkish is enough for a Turkish student in Turkey.
İngilizce Makale -1- How Can One Change?
Giving a completely or partly form or appearance to something is called as change. Developing, growing or being older are several types of change. In these days, it can be clearly seem that everything changes fast. To illustrate, the nature is damaged, people are less healthy and living is more difficult. For living in this world happily and safely, one must know she should obey this world’s rules. While the world is changing, one should change herself at the same time with it. This is true; however, do individuals of the world know how they can change themselves? Websites which include questions and chat forums about change show that especially young generation does not know clearly how they can be different. Since these websites are fulfilled with teenagers who ask about the strategies of change. One can learn the skills of change by watching two main strategies.
The first strategy for learning the skills of change is self-knowledge. Self-knowledge is being aware of what one can do, how one can develop herself/himself or what her problem is about change. When self-knowledge is thought, two major types of self-knowledge should come to minds, which are self-knowledge about failure and self-knowledge about capacity or capability. The first type of self-knowledge teaches one why s/he cannot change herself/ himself. If one knows that she does not have ability for doing something such as, passing exams, remembering telephone numbers or cooking, she will understand and solve her problems about it. Changing oneself is similar to solving these problems. Firstly, one should know why she cannot change, then, she can do the necessary activities for change. To illustrate, when a fat girl wants to be fitter, she should know why she is fat, whether she is responsible for this situation or not, she could be eating too much meat or drinking too much coke or coffee with too much sugar. After finding the causes of her situation, she may solve her problem which leads to be fitter, she can say that she changed then. Is this change? Of course, being different from her first appearance can also be included in content of change. The second type of self-knowledge is about knowing own capacities and abilities. When one knows what she can do for changing or developing herself, she can be encouraged herself for being successful about change and limiting herself to do useful activities for change. This means that, is she has information about her abilities such as cooking, make up, reading book in different languages or diving, she may develop herself easily as she does not start any strategy which she cannot do to change or develop herself. Limiting herself doing what she cannot do may make her successful in the changing process.
The second and the most important strategy for learning change is changing herself in two area. The first area of changing herself is mental change. This means that trusting herself in changing process. When one believes that she can change what she wants, this thought can motivate her starting to change. As the olders’ saying, starting is half of finishing. In addition to this, trusting herself for having ability for change may help her to be used to changes. When she is used to changes, change will be her life style. She will not stay at the same point after this process. She will want to develop herself frequently. In addition to changing herself mentally, changing herself physically is also effective for learning the skills of change. Changing physically makes one stronger and happier. Being happier and stronger makes individuals more successful in change. When one trusts that her appearance is better than past, she will be fulfilled with passion for change. As a result of this (like self-knowledge about capacity) , one feels herself motivated for developing oneself. In addition to this, her lifestyle will change with her changes too.
In conclusion, as Atatürk said, the success in civilization can only be realized by developments. In addition to this, Atatürk who was the establisher of the Turkish Republic, made changes after he had detected the situations and looked after the deficiencies of Turkey. After his observations, he made changes clearly and strongly. As Atatürk did, learning skills of change can be realized by two effective strategies: self-knowledge and changing herself.
avrupa birliği başkanlığı
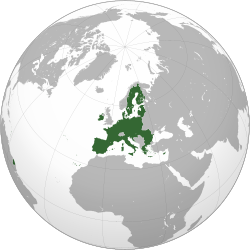
Avrupa Birliği
Vikipedi, özgür ansiklopedi
Avrupa Birliği[göster]
| ||||
|---|---|---|---|---|
| ||||
| Slogan: In varietate concordia (Latince) "Çeşitlilikte birlik"[1] | ||||
| Marş: Neşeye Övgü[1] (sözsüz) | ||||
|
| ||||
| Yönetim merkezi | Brüksel Strazburg Lüksemburg | |||
| En büyük şehir | Londra | |||
| Resmî diller | ||||
| Üye devletler | ||||
| Hükûmet | Sui generis | |||
| - | Avrupa Birliği Konseyi Başkanı | Herman Van Rompuy(AHP) | ||
| - | Avrupa Komisyonu Başkanı | José Manuel Barroso(AHP) | ||
| Kuruluş ve gelişim | ||||
| - | Paris Antlaşması | 18 Nisan 1951 | ||
| - | Roma Antlaşması | 25 Mart 1957 | ||
| - | Maastricht Antlaşması | 7 Şubat 1992 | ||
| Yüzölçümü | ||||
| - | Toplam | 4,381,376 km² (7'inci) 1,691,658 sq mi | ||
| - | Su (%) | 3.08 | ||
| Nüfus | ||||
| - | 2012 Tahminî | 503.492.041 (3'üncü) | ||
| - | Yoğunluk | 116,2/km² (93'üncü) 300.9/sq mi | ||
| GSYİH (SAGP) | 2011 (IMF) tahminî | |||
| - | Toplam | 15.821 trilyon dolar | ||
| - | Kişi başı | 31.607 dolar | ||
| GSYİH (nominal) | 2011 (IMF) Tahminî | |||
| - | Toplam | 17.577 trilyon dolar | ||
| - | Kişi başı | 35.116 dolar | ||
| Para birimi | ||||
| Zaman dilimi | (UTC+0 ila +2) | |||
| - | (Yaz saati) | (UTC+1 ila +3) | ||
| Alan adı | .eu | |||
Avrupa Birliği ya da kısaca AB, yirmi sekiz üye ülkeden oluşan ve toprakları büyük ölçüde Avrupa kıtasında bulunan siyasi ve ekonomik bir örgütlenmedir. 1992 yılında, Avrupa Birliği Antlaşması olarak da bilinen Maastricht Antlaşması'nın yürürlüğe girmesi sonucu, var olan Avrupa Ekonomik Topluluğu'na yeni görev ve sorumluluk alanları yüklenmesiyle kurulmuştur. 500 milyondan fazla nüfusuyla Avrupa Birliği, dünya ülkelerinin GSYİH’ye (nominal) göre sıralanışında nominal gayrisafi yurtiçi hasılasının %30'luk bölümünü oluşturur. (16,8 trilyon ABD$)[2]
Avrupa Birliği, tüm üye ülkeleri bağlayan standart yasalar aracılığıyla, insan, eşya, hizmet ve sermaye dolaşımı özgürlüklerini kapsayan bir ortak pazar (tek pazar) geliştirmiştir.[3] Birlik içinde tarım, balıkçılık ve bölgesel kalkınma politikalarından oluşan ortak bir ticaret politikası izlenir.[4] Birliğe üye ülkelerin on sekizi, euro adıyla anılan ortak para birimini kullanmaya başlamıştır. Avrupa Birliği, üye ülkelerini Dünya Ticaret Örgütü'nde, G8 zirvelerinde ve Birleşmiş Milletler'de temsil ederek dış politikalarında da rol oynamaktadır. Birliğin yirmi sekiz üyesinden yirmi ikisi NATO'nun da üyesidir. Schengen Antlaşmasıuyarınca birlik üyesi ülkeler arasında pasaport kontrolünün kaldırılmasının da arasında bulunduğu pek çok adlî konu ve içişileri düzenlemelerinde Avrupa Birliği'nin payı bulunur.[5]
Avrupa Birliği, devletlerarası ve çok uluslu bir oluşumdur. Birlik içinde kimi konularda devletlerarası anlaşma ve fikir birliği gerekir. Ancak belirli durumlarda uluslarüstü yönetim organları, üyelerin anlaşması olmaksızın da karara varabilir. Avrupa Birliği'nin bu tip haklara sahip önemli yönetim birimleri Avrupa Komisyonu, Avrupa Parlamentosu, Avrupa Birliği Konseyi,Liderler Zirvesi, Avrupa Adalet Divanı ve Avrupa Merkez Bankası'dır. Parlamentoyu, Avrupa Birliği vatandaşları beş yılda bir oylama yöntemiyle seçerler.
Avrupa Birliği'nin temelleri 1951 yılında, altı ülkenin katılımıyla oluşturulan Avrupa Kömür ve Çelik Topluluğu'na ve 1957 Roma Antlaşması'na dayanmaktadır. O dönemden bu yana, birlik yeni üyelerin katılımlarıyla boyut olarak büyümüş; var olan yetkilerine yeni görev ve sorumluluk alanları ekleyerek de gücünü arttırmıştır. Üye devletler Aralık 2007'de, birliğin bugüne dek yaptığı antlaşmalar ile yasal yapısını güncellemek ve iyileştirmek amacıyla Lizbon Antlaşması imzalanmıştır. Lizbon Antlaşması'nın onaylanma ve işleme girme sürecinin 2008 yılı içinde olması öngörülmüşse de İrlanda'da, antlaşmanın onaylanması için yapılan halk oylamasının ilk etapta olumsuz sonuçlanması kabul sürecini geciktirmiştir. Avrupa Birliği 2012Nobel Barış Ödülü'nü almıştır.[6]
barack obama abd başbakanı
Barack Hussein Obama (d. 4 Ağustos 1961) Amerika Birleşik Devletleri'nin devlet başkanıdır. İlk olarak 4 Kasım 2008'de yapılan2008 ABD başkanlık seçimleri'nde ABD'nin 44. devlet başkanı seçilmiş ve 20 Ocak 2009 tarihinde bu görevi George W. Bush'tan devralmıştır. 6 Kasım 2012 tarihinde yapılan 2012 ABD başkanlık seçimlerinde Mitt Romney karşısında seçimi kazanıp Amerika Birleşik Devletleri Başkanlığına ikinci kez seçilmiştir. ABD tarihindeki ilk siyahî devlet başkanıdır.
Konu başlıkları
[gizle]Yaşamı[değiştir | kaynağı değiştir]
ABD'nin Hawaii eyaletindeki Honolulu kentinde Kapiolani Tıp Merkezi'nde dünyaya geldi. Kendisiyle aynı adı taşıyan babası Kenya'nın Siaya Bölgesi'ndeki Nyang’oma Kogelo yerleşim yerinde doğmuş ve büyümüş bir Kenyalıydı. Annesi Ann Dunham ise Kansaseyaletinin Wichita kentinde doğmuş ve büyümüş bir Amerikalıydı. Obama'nın anne ve babası, babasının yabancı öğrenci olarak geldiği Hawaii'de tanıştı ve evlendi. Yeni evli çift Obama 2[1] yaşındayken boşandı. Babası Boston'a giderek Harvard Üniversitesi'nde doktora yaptı ve 1965 yılında Kenya'ya geri döndü. Annesi ise yine bir yabancı öğrenci olan Endonezyalı Lolo Soetoro'yla ikinci bir evlilik yaptı. Obama'nın hem babası, hem de üvey babası Müslüman kökenli ailelerden gelen fakat fazla dindar olmayan kişilerdi.
Annesi ve üvey babasıyla birlikte Endonezya'ya taşınan Obama 6-10 yaşları arasında Cakarta'da ilkokul öğrenimi gördü. Sonra Honolulu'ya geri dönerek 1979 yılında liseyi bitirene kadar anneannesi ve dedesiyle yaşadı. Liseden sonra Los Angeles'teki Occidental College'de üniversitenin ilk iki sınıfını okudu. Sonra New York'taki Columbia Üniversitesi'ne geçiş yaparak 1983 yılında Siyasal Bilimler bölümünden mezun oldu. 1988 yılında Harvard Üniversitesi Hukuk Fakültesi'ne girdi. Harvard Üniversitesi'ndeyken öğrenciler tarafından yayınlanan prestijli "Harvard Law Review" dergisinin yayın işleri müdürlüğünü yapan ilk Afrikalı-Amerikalı oldu. 1991 yılında avukatlık diplomasını aldı.
Obama anne ve babası boşandıktan sonra babasını sadece bir kez ABD'ye olan ziyareti sırasında 1971 yılında gördü. Yaşamının geri kalan kısmını Kenya'da geçiren babası Ruth Ndesandjo ile evlendi ve 1982 yılında Nairobi'de bir otomobil kazasında öldü. Annesi ise 1972 yılında ikinci eşinden ayrılarak Endonezya'dan ABD'ye geri döndü. 1992 yılında Hawaii Üniversitesi'nden antropoloji dalında doktora kazandı. 1995 yılında yumurtalık kanseri'nden öldü. Obama'nın anne tarafından 1 tane üvey kardeşi, baba tarafından ise 7 tane üvey kardeşi vardır.
Barack Obama 1989 yılında Michelle Robinson'la tanıştı. 3 Ekim 1992 tarihinde evlenen çift 1998 ve 2001 yıllarında doğan iki kız çocuk sahibi oldular. 1964 doğumlu Michelle Obama eşi Barack Obama gibi Harvard Üniversitesi Hukuk Fakültesi mezunu bir avukattır. Obama çifti Protestan Hristiyandır ve United Church of Christ mezhebine üyedirler.
Siyasi yaşamı[değiştir | kaynağı değiştir]
Obama avukatlık diplomasını aldıktan sonra 1992 yılından itibaren 12 yıl süreyle Chicago Üniversitesi Hukuk Fakültesinde Anayasa hukukudersleri verdi. Avukatlık firmalarında çalıştı, çeşitli yardım dernekleri ve vakıflarda görev yaptı. 1996 yılında İllinois'in eyalet senatosuna seçilerek siyasete ilk adımını attı. 1998 ve 2002 yıllarında iki kez tekrar eyalet senatosuna seçildi. 2000 yılında ABD Temsilciler Meclisi'ne girmek için Demokratik Partinin ön seçimlere katıldı ama başarılı olamadı. 2004 tarihinde adaylığını koyduğu ABD Senatosu'nuna % 70'lik bir oy çoğunluğu almak suretiyle seçildi.
Obama'nın ABD'de ilk defa ülke sahnesine çıkması 2004 ABD başkanlık seçimleri sırasında Boston'da toplanan Demokratik Parti kurultayında yaptığı ve ülke çapında televizyonda canlı olarak yayınlanan etkileyici konuşması sayesinde olmuştur. Obama Senato'daki hizmet döneminde Senato Dışişleri Komisyonunda görev yaptı. Doğu Avrupa, Orta Doğu, Orta Asya ve Afrika'ya resmi ziyaretlerde bulundu. Filistincumhurbaşkanı Mahmud Abbas'la buluştu. Kenya'da Nairobi Üniversitesi'nde bir konferans verdi. ABD Senatosu'nda henüz 6 yıllık ilk dönemini tamamlamamışken 10 Şubat 2007 tarihinde 2008 ABD başkanlık seçimlerine Demokratik Parti'den adaylığını koyduğunu açıkladı[2].
2008 ABD başkanlık seçimleri[değiştir | kaynağı değiştir]
- Ana madde: 2008 ABD başkanlık seçimleri
Barack Obama'nın yanı sıra Demokratik Parti içindeki başkanlık ön seçimlerine adaylığı koyan siyasetçiler arasında Hillary Clinton,John Edwards, Joe Biden, Christopher Dodd ve Bill Richardson gibi birçok tanınmış siyasetçiler bulunmaktaydı. Özellikle aday adayları arasındaki New York senatörü Hillary Clinton eski ABD başkanı Bill Clinton'un eşi olarak çok tanınmış bir siyasetçiydi ve 2007 yılı boyunca Demokratik Parti içinde en şanslı aday olarak görülmekteydi.

Joe Biden ve Barack Obama bir seçim mitinginde
ABD başkanlık seçimleri'nde iki büyük partiyi temsil edecek başkan adayı her eyalette ayrı ayrı ve değişik tarihlerde yapılan ön seçimlerle belirlenmektedir. Bu ön seçimlerden ilkiIowa eyaletinde 3 Ocak 2008 tarihinde gerçekleşti. Zencilerin sayısının çok az olduğu bu eyalette Barack Obama'nın beklenmedik bir başarı elde ederek seçimi kazanması Hillary Clinton'un adaylık şansını olumsuz yönde etkiledi. Ancak Clinton 5 gün sonra New Hampshire eyaletindeki seçimleri kazanarak yarışı sürdürdü. 2008'in Ocak ayı boyunca Demokratik Parti içinde Hillary Clinton ve Barack Obama dışındaki bütün adaylar birer birer adaylıktan çekildiklerini ilan ettiler.
Ön seçim takvimine göre 5 Şubat 2008 günü 20 eyalette aynı anda yapılacak Süper Salı seçimleri kritik bir önem taşımaktaydı. Ancak Süper Salı gününde kazanılan oylar iki aday arasında eşitliği bozmadı. Ön seçimler diğer eyaletlerde devam etti. Zamanla Obama'nın Clinton'a kıyasla az bir farkla öne geçtiği gözlendi. Buna rağmen Haziran ayına kadar adaylık yarışı başa baş devam etti. Hillary Clinton Obama'yı sonuna kadar az bir farkla takip ediyordu. Ancak ön seçimler 3 Haziran 2008 tarihinde South Dakota ve Montanaeyaletleriyle tamamlandıktan sonra Hillary Clinton'un Obama'nın açtığı bu küçük farkı kapatamayacağı anlaşıldı. Barack Obama Demokratik Parti'nin 2008 ABD başkanlık seçimlerindeki adayı olarak ilan edildi. Böylece Obama ABD tarihinde iki büyük partinin birinden aday gösterilmiş ilk Afrikalı-Amerikalı aday olma özelliğini kazanmış oldu.
Demokratik Partinin kurultayı 25-28 Ağustos 2008 tarihleri arasında Colorado eyaletinin Denver kentindeki Pepsi Center'da yapıldı[3]. Barack Obama 28 Ağustos gecesi canlı yayınla aktarılan konuşmasında Demokratik Parti'nin adaylığını resmen kabul etti. 1 hafta sonra Minnesota eyaletinin St. Paul kentindeki XCel Energy Center'da yapılan Cumhuriyetçi Parti kurultayında Arizona senatörü John McCain'in başkan adaylığını onaylandı[4]. Böylece 2008 ABD başkanlık seçimleri kampanyası resmen başlamış oldu.
Barack Obama ve John McCain 26 Eylül- 15 Ekim tarihleri arasında televizyon kameraları önünde 3 defa münazara yaptılar. Seçim kampanyası sırasında ABD gündemi 2008 Ekonomik Kriziylesarsıldı. Irak Savaşı ve Terörizm gibi konular arka plana itildi. Obama McCain'in Cumhuriyetçi Partili başkan George W. Bush'un başarısız ekonomik siyasetlerini devam ettireceğini öne sürdü. McCain ise Obama'nın küçük esnafın gelir vergilerini arttıracağını iddia etti. Seçim kampanyası süresince Obama hakkında birçok iddia dile getirilmiştir[5].
2008 ABD başkanlık seçimleri 4 Kasım 2008 günü yapıldı. Barack Obama oyların %52'sini kazanarak ABD'nin 44. devlet başkanı seçildi. Obama kazandığı oy oranı ve kazandığı eyaletler bakımından son 30 yıl boyunca hiçbir Demokrat Partili başkan adayının elde edemediği bir başarıyı elde etmiştir. Obama'nın adaylığı altında Demokrat Parti Virginia, Florida ve Ohio gibi son seçimlerde değişmez bir biçimde Cumhuriyetçilere oy veren eyaletleri kazanmayı başarabilmiştir. Seçim zaferi sonrasında yaptığı konuşmada Obama, ABD'nin gelecek döneminde zorlukların ve hataların olabileceğini belirtmiş, yaşanacak sıkıntıların ise vatanseverlikle aşılacağını anlatmıştır[6].
Barack Obama 20 Ocak 2009 günü yerel saatle 12.00 (TSİ 19.00)'de daha önce 1861 yılında başkan Abraham Lincoln'un yemin töreninde kullandığı incil'e el basıp yemin ederekGeorge W. Bush'tan görevi devraldı ve Resmen ABD devlet başkanı oldu.
2012 ABD başkanlık seçimleri[değiştir | kaynağı değiştir]
- Ana madde: 2012 ABD başkanlık seçimleri
Bu seçimlerde Demokratik Parti'yi 2008 yılında ilk kez ABD başkanı seçilmiş olan Barack Obama temsil ederken, Cumhuriyetçi Parti'yi ise eski Massachusetts eyaleti valisi ve iş adamı Mitt Romney temsil etti. Seçimi kazanmayı başaran Barack Obama tekrar ikinci bir kez 4 yıl süreyle ABD başkanlığı görevini üstlendi.
Kronoloji[değiştir | kaynağı değiştir]
- 4 Ağustos 1961 tarihinde ABD'nin Hawaii eyaletindeki Honolulu kentinde dünyaya geldi.
- 1967-1971 yılları arasında Endonezya'nın Cakarta kentinde yaşadı.
- 1971-1979 yılları arasında Honolulu'da yaşadı.
- 1983'te New York'taki Columbia Üniversitesi Siyasal Bilimler Fakültesinden mezun oldu.
- 1983-1987 yılları arasında New York'ta yaşadı.
- 1991 yılında Harvard Üniversitesinden avukatlık diplomasını aldı.
- 1996 İllinois eyalet senatosuna seçildi.
- 2 Kasım 2004'te ABD Senatosuna seçildi.
- 10 Şubat 2007'de İllinois eyaletinin Springfield kentinde ABD başkanlığına adaylığını koydu.
- 3 Haziran 2008'de Demokratik Parti'nin ön seçimlerini kazandığı kesinleşti.
- 25 Temmuz 2008 Dış politika önceliklerini desteklemeyi amaçlayan uluslararası gezisinin son ayağı için Almanya'ya gitti[7]. Yaklaşık 200.000 kişiye hitap eden Barack Obama'nın Almanya'da yaptığı konuşmadan: "Irklar ve toplumlar; yerliler ve göçmenler; Hıristiyanlar ve Müslümanlar ve Yahudiler arasındaki duvarlar daha fazla dikilmeye devam edemez. Bunlar şimdi yıkılmak zorunda olan duvarlardır."[8]
- 27 Temmuz 2008 ABD başkan adayı Barack Obama İngiltere’yi ziyaret ettiği sırada, Berkshire’deki evinde ulaşılan Müslüman üvey kardeşi Bernard Obama, "Kardeşimle gurur duyuyorum." dedi.Kenya’nın başkenti Nairobi’de sahibi olduğu mağazada oto parçaları sattığını belirten Bernard, "Sık sık gelirim" dediği İngiltere’de, sosyal konutlarda annesi Kezia (67) ile birlikte oturuyor. Bernard, "İlk kez 17 yaşındayken Barack ile karşılaştım. Babam Müslüman’dı ben de 18 yıl önce Müslümanlığı seçtim. Barack ise Hıristiyandır" dedi.[9]
- 30 Temmuz 2008 CNN'de yayınlanan 28 Temmuz'da yapılan anket sonuçlarına göre Obama %45, McCain %40[10][11].
- 25 Ağustos 2008, Denver'de toplanan Demokratik Parti kurultayı resmen Barack Obama'nın başkan adaylığını onayladı.
- 26 Eylül 2008, Oxford, Missisippi'de Barack Obama ve McCain ilk münazaralarını yaptılar.
- 8 Ekim 2008, kamuoyu yoklamaları Obama'nın tekrar öne geçtiğini gösteriyor[12].
- 4 Kasım 2008, 2008 ABD başkanlık seçimleri'nde ABD'nin 44. devlet başkanı seçildi.
- 20 Ocak 2009'da yemin ederek resmen ABD Başkanı oldu.
Kaydol:
Kayıtlar (Atom)